|
||||||||||||
|
|
||||||||||||
 |
|
|
|
|
Lautenbach - Stuttgart: Nun ist sie wieder da die langersehnte, heimische Erdbeere. Wenn auch der diesjährige Frost den Erdbeeren im Südwesten teilweise arg zugesetzt hat, haben die Erdbeeren aus Baden-Württemberg, trotz reduzierter Mengen, eine hervorragende Qualität. Erdbeeren sind ein sehr bekömmliches und gesundes Lebensmittel. Sie sind ein idealer Schlankmacher, enthalten viel Wasser und kaum Kalorien und haben mehr Vitamin C als Zitronen und Orangen, so dass mit nur 120g Erdbeeren der Tagesbedarf an Vitamin C gedeckt ist. Folsäure und Mineralstoffe wie Kalium und Magnesium stärken das Herz. |
 |
 |
 |
|||||
|
Unsere Fotos zeigen: Die vom Frost nicht zerstörten Erdbeeren werden von fleißigen Helfern geerntet - so wie hier auf der Erdbeerplantage Hofladen Linckh aus Vaihingen/Enz |
|||||||
|
Zum Start der Erdbeersaison in Baden-Württemberg möchten wir die Verbraucherinnen und Verbraucher ermuntern, gezielt heimische Erdbeeren nachzufragen. Dank sonniger Lagen, fruchtbarer Böden und hochqualifizierter |
|
|
|
|
|
Rund jede fünfte in Deutschland erzeugte Erdbeere stamme aus Baden-Württemberg. Mit einer Menge von rund 26.000 Tonnen habe Baden-Württemberg im Jahr 2016 nach Niedersachsen und Nordrhein-Westfalen bundesweit auf Platz drei der Erdbeer-Erzeuger gelegen. Text und Foto: POSITIV-MEDIEN (PR-mlr-bw * Hofladen-Linckh * Waldemar Herzog) |
|
|
|
Stuttgart: Nachdem mit Hamburg eine weitere Großstadt Fahrverbote für ältere Dieselfahrzeuge angekündigt hat, fordert der ACE dringend eine schnelle Reaktion der Fahrzeughersteller und der Politik. Die derzeitige Situation in Deutschland lässt vermuten, dass das Bundesverkehrsministerium und die Autoindustrie das Problem der Luftschadstoffe aussitzen wollen, so Stefan Heimlich, Vorsitzender des zweitgrößten deutschen Autoclubs. |
 |
|
Unumstritten ist, dass auch Neufahrzeuge zu viele Schadstoffe ausstoßen und dass besser kontrolliert werden muss. Trotzdem sprechen sich Hersteller sowohl gegen eine europaweite Überwachung als auch gegen verschärfte Sanktionen aus. Für uns ist das unverständlich: Die deutschen Autohersteller haben das Fachwissen, saubere Fahrzeuge zu bauen, und solche Maßnahmen würden das Vertrauen der Menschen in die Fahrzeugindustrie deutlich erhöhen, so der ACE-Vorsitzende. Auch beim Nachrüsten älterer Fahrzeuge vermisst der ACE ein entschiedenes Handeln. Der ACE unterstützt hier deutlich die Position des Bundes-umweltministeriums, dass Hersteller und Zulieferer schnelle und pragmatische Lösungen anbieten müssen. Die ACE-Forderung ist, dass wir neben sauberen Neufahrzeugen sozial verträgliche Übergangslösungen brauchen. Nicht jedes ältere Dieselfahrzeug wird durch eine Nachrüstung den neusten Standard erreichen können. Aber jede Nachrüstung trägt ein Stück weit zur sauberen Luft in unseren Städten bei und nachgerüstete Fahrzeuge könnten deswegen von Fahrverboten ausgenommen werden. Erste Lösungen aus der Schweiz liegen vor. Wo bleibt die deutsche Industrie? Angesichts der drohenden Fahrverbote müssen die Hersteller zusammen mit dem Verkehrsministerium schnell aktiv werden. Nur so können Kommunen bei der Lösung der Schadstoffprobleme unterstützt werden. Bleibt diese Unterstützung aus, liegt die Verantwortung für daraus folgende Wertverluste und Mobilitätseinschränkungen klar bei der Fahrzeugindustrie und dem für Zulassungen zuständigen Ministerium so Stefan Heimlich. Text und Foto: POSITIV-MEDIEN (PR-ACE * Emmerling * Waldemar Herzog) |
|
|
|
Ludwigsburg: Unter dem Motto Zeit zu zweit lädt der Pflegestützpunkt Stadt Ludwigsburg Menschen mit Demenz zusammen mit einer vertrauten Person aus der Familie am Dienstag, den 09. Mai 2017, um 14:00 Uhr, zu einem gemütlichen Spaziergang am Seeschloss Monrepos (Foto-unten-links) ein. |
 |
 |
|
Die gemeinsame Bewegung auf dem Spazierpfad rund um den See sind ebenso wie die netten Gespräche eine Wohltat für Körper und Geist. Treffpunkt ist die Bushaltestelle Seeschloss Monrepos. Im Anschluss besteht die Möglichkeit, gemeinsam im Restaurant La Corte den Nachmittag in geselliger Runde ausklingen zu lassen. Begleitet wird die Gruppe von Mitarbeiterinnen des Pflegestützpunktes. Die Rahmenbedingungen sind an die Bedürfnisse von Menschen mit Demenz angepasst. Neue Familien sind herzlich willkommen. |
|
Weitere Informationen und Anmeldung im Pflegestützpunkt:Telefon 07141- 9103123 * Email: pflegestuetzpunkt@ludwigsburg.de * Internet:www.ludwigsburg.de/pflegestuetzpunkt * |
|
Text und Foto: POSITIV-MEDIEN (PR-Stadt-LB * Waldemar Herzog) |
|
|
|
|
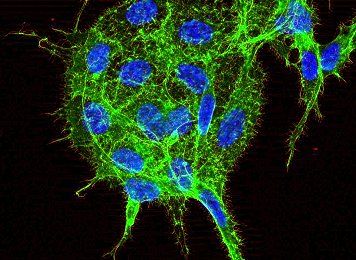
Freiburg: Ein internationales Team um Dr. Florian Weinberg aus der Gruppe von Prof. Dr. Tilman Brummer vom Institut für Molekulare Medizin und Zellforschung (IMMZ) der Universität Freiburg, der klinischen Pathologie und Medizin I des Universitätsklinikums und dem Kinghorn Cancer Centre/Garvan Insitute in Australien hat einen neuen Ansatz gefunden, mit dem sich das Tumorwachstum bei Krebserkrankungen möglicherweise stoppen lässt. |
|
|
|
Mithilfe so genannter Inhibitoren könnte es gelingen, die Enzymaktivität von RIOK1 zu hemmen und das Fortschreiten der Erkrankung einzudämmen. Das Team veröffentlichte seine Resultate im Fachjournal EBioMedicine. Krebserkrankungen sind durch Genmutationen charakterisiert, welche unkontrolliertes Wachstum körpereigener Zellen zur Folge haben und so zur Tumorentstehung führen. Die meisten Behandlungen kombinieren operative Eingriffe, um dem Tumor zu entfernen, mit Chemo- oder Strahlentherapie, die beide darauf abzielen, schnell wachsende Zellen zu hemmen. Als Ergänzung oder Alternative kommen spezifische Inhibitoren zum Einsatz. Diese Wirkstoffe hemmen die Aktivität von schädlichen Proteinen und Enzymen, die durch im Tumor mutierte Gene produziert werden. Speziell für 2 RAS-getriebene Tumore gibt es jedoch bislang nur mangelnde Behandlungsmöglichkeiten. Von solchen Tumoren sind etwa 30 Prozent aller Krebspatienten betroffen. Daher ist es von großem Interesse, neue Wege zu finden, um auf RAS einzuwirken. Die Forscher untersuchten unter anderem das Wachstumsverhalten von AS-mutierten menschlichen Lungen-, Brust-, und Darmkrebszellen mittels Zellkultur- und Tiermodellen. Es gelang ihnen jeweils, diese Zellen genetisch so zu verändern, dass sie nicht mehr in der Lage waren, RIOK1 zu produzieren. Mit diesem Ansatz, der die Effekte eines RIOK1-Inhibitors nachahmt, verringerten sie das Wachstum und die Aggressivität der Krebszellen. Besonders bei den Tiermodellen beobachteten die Forscher, dass die veränderten Zellen nicht mehr in der Lage waren, Metastasen zu bilden. RIOK1 gehört zu den Proteinkinnasen, einer Familie von Enzymen, die in der Krebstherapie mittels Inhibitoren bereits oft erfolgreich gehemmt werden. Daher nehmen die Forscher an, dass ähnliche Hemmstoffe, welche die Enzymaktivität von RIOK1 unterbinden, in absehbarer Zeit entwickelt werden könnten. Zusätzlich könnte RIOK1 ermöglichen, den weiteren Verlauf von Lungen- und Brustkrebserkrankungen besser vorherzusagen: Die Forscher beobachteten bei Patienten mit schlechteren Prognosen eine verstärkte Produktion von RIOK1 im Tumorgewebe. Allerdings werden den Forschern zufolge weitere Arbeiten nötig sein, um RIOK1 als eine Zielstruktur für die Krebstherapie zu bestätigen. Wichtig sei etwa, den genauen Mechanismus aufzuklären, wie das Enzym Krebswachstum und Metastasierung fördert. Zudem sei es unumgänglich, Inhibitoren an Modellorganismen zu testen, bevor die Wirkstoffe in klinischen Studien erprobt werden können. Erste Untersuchungen der Forscher an Fadenwürmern und menschlichen Zellen haben gezeigt, dass gesunde Körperzellen nicht oder nur teilweise von einem RIOK1-Verlust betroffen sind, weil diese nicht auf das Enzym angewiesen sind. Dagegen wären Krebszellen in ihrem Wachstum und in ihrer Fähigkeit, neue Tumore zu streuen, gehemmt. Hintergrund: Die Albert-Ludwigs-Universität Freiburg erreicht in allen Hochschulrankings Spitzenplätze. Forschung, Lehre und Weiterbildung wurden in Bundeswettbewerben prämiert. 25.000 Studierende aus über 100 Nationen sind in 197 Studiengängen eingeschrieben. Etwa 6.000 Lehrkräfte sowie Mitarbeiterinnen und Mitarbeiter in der Verwaltung engagieren sich und erleben, dass Familienfreundlichkeit, Gleichstellung und Umweltschutz hier ernst genommen werden. Text und Foto: POSITIV-MEDIEN (PR-ALUni-Freiburg * Waldemar Herzog) |
|
|
|
Der kleine Gladiator mit dem Schleuderschwanz |
|
Jetzt ist auch für ihn die Winterpause vorbei: Auftritt für den Hardun! Jeden Tag brandet Applaus an seinem Gehege in der Wilhelma auf. Doch gelten die Ovationen nie der kleinen Echse. Ihre Bühne ist nur Nebenschauplatz, wenn die Besucher das Seelöwenbecken bei der Fütterung zu Hunderten umringen und dem Hardun den Rücken zukehren. Und so lebt an prominenter Stelle des Zoologisch-Botanischen Gartens in Stuttgart ein unter den Wilhelma-Tieren wenig bekannter Charakter, der dennoch absolut sehenswert ist. Dabei fristet er keineswegs ein Schattendasein, sondern lässt sich an einem der sonnigsten Orte des Parks als wechselwarmes Reptil von den wärmenden Strahlen auf Betriebstemperatur bringen. |
 |
 |
||||||||
 |
 |
||||||||
|
Unsere Fotos zeigen: Ein Hardun auf der mediterranen Außenanlage der Wilhelma in Stuttgart zeigt im Frühjahr blaue Einsprengsel in seiner ansonsten graubraunen Färbung. |
|||||||||
|
Der Hardun ist etwas Besonderes. Unter den Schuppenkriechtieren zählt er zu der Familie der Agamen. Deren 280 Arten sind anpassungsfähig und von Nordafrika über Südwestasien bis nach Australien anzutreffen. Nur in Europa gibt es lediglich eine einzige Agamen-Art: den Hardun. Ihn findet man auf Inseln in der Ägäis wie Kos, Samos oder Rhodos bis nach Saloniki auf dem griechischen Festland sowie in der Türkei. In der Wilhelma bewohnt er daher mit den Griechischen Landschildkröten, Breitrandschildkröten, Perleidechsen und der Schleichen-Art Scheltopusik die mediterrane Landschaft vor der Krokodilhalle. In die Nachbarschaft passt er auch optisch gut. Beschuppt und stachelig erinnert sein wehrhaftes Erscheinungsbild an die Krokodile selbst wenn er nur eine Körperlänge von bis zu 35 Zentimetern erreicht. Und zu der trägt bereits erheblich sein martialisch aussehender Schwanz bei: Stachelbewehrt und sehr hart hat ihm diese Waffe den Beinamen Schleuderschwanz eingetragen. Dabei ist das scheue Tier nicht kämpferisch, es flüchtet sich bei Gefahr in Felsspalten. Doch dringt ein Feind weiter vor, dreht sich der kleine Gladiator schnell im Kreis und schleudert so seinen Schwanz herum, um den Eindringling zu treffen. Ab Oktober waren die Reptilien vor Frost geschützt in ihrem Winterquartier. Seit der Frühling milder geworden ist, konnten die Sonnenanbeter auf ihre Außenanlage zurückkehren. Aktuell lohnt ein genauerer Blick. Denn nach der Winterruhe beginnt gleich die Paarungszeit. Dann zeigt das sonst graubraune bis schwarze Hardun-Männchen blaue Einsprengsel. Zu beobachten ist auch das auffällige Kopfnicken. Es dient dem Sozialverhalten mit Artgenossen: dem Drohen und Dominieren gegenüber anderen Männchen, aber auch dem Imponieren und Balzen gegenüber Weibchen. Text und Foto: POSITIVMEDIEN (PR-Wilhelma * Waldemar Herzog) |
|||||||||
 |
|||||||||